
Top ▲

GtoPdb is requesting financial support from commercial users. Please see our sustainability page for more information.
| Quaternary Structure: Subunits |
| 5-HT3A |
Selected 3D Structures  |
|||||||||||
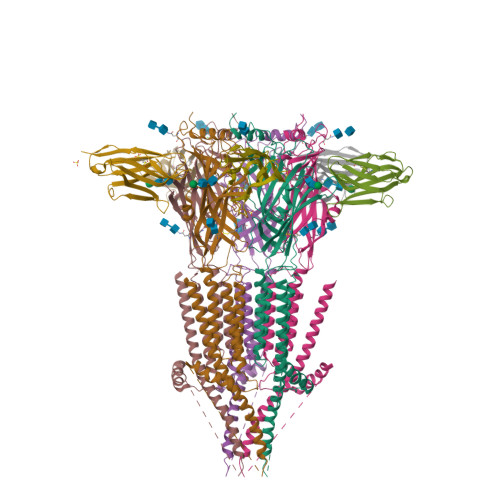
|
|
||||||||||
Ion Selectivity and Conductance  |
|||||||||
|
|||||||||
|
|||||||||
|
|||||||||
|
|||||||||
| Ion Selectivity and Conductance Comments | |||||||||
| For the human receptor PCa/PCs = 1.0-1.4 [5,11,35] and PMg/PCs = 0.41-0.61 [5,11]. The fractional calcium flux (Ca2+ Pf) is 4.1% [45]. |
Natural/Endogenous Ligands  |
| Ca2+ |
| 5-hydroxytryptamine |
| Mg2+ |
| Zn2+ |
Download all structure-activity data for this target as a CSV file 
| Agonists | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Key to terms and symbols | View all chemical structures | Click column headers to sort | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| View species-specific agonist tables | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Agonist Comments | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apparent affinities of agonists are for ligand binding to the recombinant 5-HT3A receptor expressed in mammalian cells, or pEC50 values determined under voltage-clamp for the receptor expressed in Xenopus laevis oocytes. Selectivity refers to the 5-HT3 receptor family: the agents listed do not discriminate between 5-HT3A and 5-HT3AB receptors, although their affinities/potencies at the latter are in some cases lower. Comments concerning efficacy relate to data obtained from voltage-clamp studies of, where possible, the relevant species orthologues of 5-HT3A receptor expressed in Xenopus laevis oocytes [2,36,50]. Where significant species differences in agonist potency exist, data for rat and mouse orthologues of the receptor are also listed. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Antagonists | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Key to terms and symbols | View all chemical structures | Click column headers to sort | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| View species-specific antagonist tables | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Antagonist Comments | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Data tabulated are for ligand binding to the recombinant 5-HT3A receptor expressed in mammalian cells. Selectivity refers to the 5-HT3 receptor family: the agents listed no not discriminate between 5-HT3A and 5-HT3AB receptors in radioligand binding assays. In electrophysiological studies, (+)-tubocurarine demonstrates modest selectivity for human 5-HT3A (IC50 = 3 μM) versus human 5-HT3AB (IC50 = 14 – 21 μM) receptors [11]. Where significant species differences in antagonist affinity exist, data for the mouse orthologue of the receptor are also listed. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Channel Blockers | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Key to terms and symbols | View all chemical structures | Click column headers to sort | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| View species-specific channel blocker tables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Channel Blocker Comments | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Although picrotoxin is approximately 27-fold more potent in blocking mouse 5-HT3A versus mouse 5-HT3AB receptors, the degree of discrimination between the equivalent human receptor orthologues is likely to be substantially smaller due to differences in the structure of the TM2 domain [10]. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Allosteric Modulators | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Key to terms and symbols | View all chemical structures | Click column headers to sort | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| View species-specific allosteric modulator tables | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Allosteric Modulator Comments | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numerous positive modulators of the 5-HT3A receptor exist, but most also exert effects at other ligand-gated ion channels. Only the most extensively characterised are listed above together with an indication of the range of concentrations over which they modulate submaximal inward currents evoked by 5-HT acting on either mouse of human 5-HT3A receptors expressed in Xenopus laevis oocytes or HEK-293 cells, or 5-HT3 receptors endogenous to clonal cell lines (which are likely to be homomeric 5-HT3A receptors). Chloroform, halothane and small volume n-alcohols enhance the gating of 5-HT3A receptors and incorporation of the 5-HT3B subunit to form 5-HT3AB receptors suppresses this action [49-50]. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Functional Assays 
|
||||||||||
|
||||||||||
|
||||||||||
|
||||||||||
|
||||||||||
|
||||||||||
|
||||||||||
|
1. Abi-Dargham A, Laruelle M, Wong DT, Robertson DW, Weinberger DR, Kleinman JE. (1993) Pharmacological and regional characterization of [3H]LY278584 binding sites in human brain. J Neurochem, 60 (2): 730-7. [PMID:8419547]
2. Belelli D, Balcarek JM, Hope AG, Peters JA, Lambert JJ, Blackburn TP. (1995) Cloning and functional expression of a human 5-hydroxytryptamine type 3AS receptor subunit. Mol Pharmacol, 48 (6): 1054-62. [PMID:8848005]
3. Bonhaus DW, Stefanich E, Loury DN, Hsu SA, Eglen RM, Wong EH. (1995) Allosteric interactions among agonists and antagonists at 5-hydroxytryptamine3 receptors. J Neurochem, 65 (1): 104-10. [PMID:7790853]
4. Brady CA, Stanford IM, Ali I, Lin L, Williams JM, Dubin AE, Hope AG, Barnes NM. (2001) Pharmacological comparison of human homomeric 5-HT3A receptors versus heteromeric 5-HT3A/3B receptors. Neuropharmacology, 41 (2): 282-4. [PMID:11489465]
5. Brown AM, Hope AG, Lambert JJ, Peters JA. (1998) Ion permeation and conduction in a human recombinant 5-HT3 receptor subunit (h5-HT3A). J Physiol (Lond.), 507 ( Pt 3): 653-65. [PMID:9508827]
6. Brüss M, Molderings GJ, Bönisch H, Göthert M. (1999) Pharmacological differences and similarities between the native mouse 5-HT3 receptor in N1E-115 cells and a cloned short splice variant of the mouse 5-HT3 receptor expressed in HEK 293 cells. Naunyn Schmiedebergs Arch Pharmacol, 360 (3): 225-33. [PMID:10543422]
7. Dang H, England PM, Farivar SS, Dougherty DA, Lester HA. (2000) Probing the role of a conserved M1 proline residue in 5-hydroxytryptamine(3) receptor gating. Mol Pharmacol, 57 (6): 1114-22. [PMID:10825381]
8. Das P, Bell-Horner CL, Machu TK, Dillon GH. (2003) The GABA(A) receptor antagonist picrotoxin inhibits 5-hydroxytryptamine type 3A receptors. Neuropharmacology, 44 (4): 431-8. [PMID:12646280]
9. Das P, Dillon GH. (2003) The 5-HT3B subunit confers reduced sensitivity to picrotoxin when co-expressed with the 5-HT3A receptor. Brain Res Mol Brain Res, 119 (2): 207-12. [PMID:14625088]
10. Das P, Dillon GH. (2005) Molecular determinants of picrotoxin inhibition of 5-hydroxytryptamine type 3 receptors. J Pharmacol Exp Ther, 314 (1): 320-8. [PMID:15814570]
11. Davies PA, Pistis M, Hanna MC, Peters JA, Lambert JJ, Hales TG, Kirkness EF. (1999) The 5-HT3B subunit is a major determinant of serotonin-receptor function. Nature, 397 (6717): 359-63. [PMID:9950429]
12. Downie DL, Hope AG, Belelli D, Lambert JJ, Peters JA, Bentley KR, Steward LJ, Chen CY, Barnes NM. (1995) The interaction of trichloroethanol with murine recombinant 5-HT3 receptors. Br J Pharmacol, 114 (8): 1641-51. [PMID:7541281]
13. Downie DL, Hope AG, Lambert JJ, Peters JA, Blackburn TP, Jones BJ. (1994) Pharmacological characterization of the apparent splice variants of the murine 5-HT3 R-A subunit expressed in Xenopus laevis oocytes. Neuropharmacology, 33 (3-4): 473-82. [PMID:7984286]
14. Dubin AE, Huvar R, D'Andrea MR, Pyati J, Zhu JY, Joy KC, Wilson SJ, Galindo JE, Glass CA, Luo L et al.. (1999) The pharmacological and functional characteristics of the serotonin 5-HT(3A) receptor are specifically modified by a 5-HT(3B) receptor subunit. J Biol Chem, 274 (43): 30799-810. [PMID:10521471]
15. Edwards E, Hampton E, Ashby CR, Zhang J, Wang RY. (1996) 5-HT3-like receptors in the rat medial prefrontal cortex: further pharmacological characterization. Brain Res, 733 (1): 21-30. [PMID:8891244]
16. Gill CH, Peters JA, Lambert JJ. (1995) An electrophysiological investigation of the properties of a murine recombinant 5-HT3 receptor stably expressed in HEK 293 cells. Br J Pharmacol, 114 (6): 1211-21. [PMID:7620711]
17. Gunthorpe MJ, Lummis SC. (1999) Diltiazem causes open channel block of recombinant 5-HT3 receptors. J Physiol (Lond.), 519 Pt 3: 713-22. [PMID:10457085]
18. Hales TG, Dunlop JI, Deeb TZ, Carland JE, Kelley SP, Lambert JJ, Peters JA. (2006) Common determinants of single channel conductance within the large cytoplasmic loop of 5-hydroxytryptamine type 3 and alpha4beta2 nicotinic acetylcholine receptors. J Biol Chem, 281 (12): 8062-71. [PMID:16407231]
19. Hargreaves AC, Lummis SC, Taylor CW. (1994) Ca2+ permeability of cloned and native 5-hydroxytryptamine type 3 receptors. Mol Pharmacol, 46 (6): 1120-8. [PMID:7808432]
20. Hassaine G, Deluz C, Grasso L, Wyss R, Tol MB, Hovius R, Graff A, Stahlberg H, Tomizaki T, Desmyter A et al.. (2014) X-ray structure of the mouse serotonin 5-HT3 receptor. Nature, 512 (7514): 276-81. [PMID:25119048]
21. Hayrapetyan V, Jenschke M, Dillon GH, Machu TK. (2005) Co-expression of the 5-HT(3B) subunit with the 5-HT(3A) receptor reduces alcohol sensitivity. Brain Res Mol Brain Res, 142 (2): 146-50. [PMID:16257471]
22. Hirata T, Keto Y, Funatsu T, Akuzawa S, Sasamata M. (2007) Evaluation of the pharmacological profile of ramosetron, a novel therapeutic agent for irritable bowel syndrome. J Pharmacol Sci, 104 (3): 263-73. [PMID:17652911]
23. Hope AG, Peters JA, Brown AM, Lambert JJ, Blackburn TP. (1996) Characterization of a human 5-hydroxytryptamine3 receptor type A (h5-HT3R-AS) subunit stably expressed in HEK 293 cells. Br J Pharmacol, 118 (5): 1237-45. [PMID:8818349]
24. Hu XQ, Hayrapetyan V, Gadhiya JJ, Rhubottom HE, Lovinger DM, Machu TK. (2006) Mutations of L293 in transmembrane two of the mouse 5-hydroxytryptamine3A receptor alter gating and alcohol modulatory actions. Br J Pharmacol, 148 (1): 88-101. [PMID:16520747]
25. Hu XQ, Lovinger DM. (2005) Role of aspartate 298 in mouse 5-HT3A receptor gating and modulation by extracellular Ca2+. J Physiol (Lond.), 568 (Pt 2): 381-96. [PMID:16096341]
26. Hu XQ, Peoples RW. (2008) Arginine 246 of the pretransmembrane domain 1 region alters 2,2,2-trichloroethanol action in the 5-hydroxytryptamine3A receptor. J Pharmacol Exp Ther, 324 (3): 1011-8. [PMID:18094321]
27. Hu XQ, Peoples RW. (2008) The 5-HT3B subunit confers spontaneous channel opening and altered ligand properties of the 5-HT3 receptor. J Biol Chem, 283 (11): 6826-31. [PMID:18187416]
28. Hubbard PC, Lummis SC. (2000) Zn(2+) enhancement of the recombinant 5-HT(3) receptor is modulated by divalent cations. Eur J Pharmacol, 394 (2-3): 189-97. [PMID:10771284]
29. Hussy N, Lukas W, Jones KA. (1994) Functional properties of a cloned 5-hydroxytryptamine ionotropic receptor subunit: comparison with native mouse receptors. J Physiol (Lond.), 481 ( Pt 2): 311-23. [PMID:7537814]
30. Ito H, Kiso T, Miyata K, Kamato T, Yuki H, Akuzawa S, Nagakura Y, Yamano M, Suzuki M, Naitoh Y et al.. (2000) Pharmacological profile of YM-31636, a novel 5-HT3 receptor agonist, in vitro. Eur J Pharmacol, 409 (2): 195-201. [PMID:11104834]
31. Kelley SP, Dunlop JI, Kirkness EF, Lambert JJ, Peters JA. (2003) A cytoplasmic region determines single-channel conductance in 5-HT3 receptors. Nature, 424 (6946): 321-4. [PMID:12867984]
32. Kooyman AR, van Hooft JA, Vijverberg HP. (1993) 5-Hydroxyindole slows desensitization of the 5-HT3 receptor-mediated ion current in N1E-115 neuroblastoma cells. Br J Pharmacol, 108 (2): 287-9. [PMID:7680589]
33. Lankiewicz S, Lobitz N, Wetzel CH, Rupprecht R, Gisselmann G, Hatt H. (1998) Molecular cloning, functional expression, and pharmacological characterization of 5-hydroxytryptamine3 receptor cDNA and its splice variants from guinea pig. Mol Pharmacol, 53 (2): 202-12. [PMID:9463477]
34. Lee BH, Choi SH, Pyo MK, Shin TJ, Hwang SH, Kim BR, Lee JH, Rhim H, Kim HC, Nah SY. (2009) A role for the Val291 residue within the transmembrane domain 2 in diltiazem- and TMB-8 [3,4,5-trimethoxybenzoic acid 8-(diethylamino)octyl ester]-mediated 5-hydroxytryptamine type 3A receptor regulations. Biol Pharm Bull, 32 (5): 861-7. [PMID:19420755]
35. Livesey MR, Cooper MA, Deeb TZ, Carland JE, Kozuska J, Hales TG, Lambert JJ, Peters JA. (2008) Structural determinants of Ca2+ permeability and conduction in the human 5-hydroxytryptamine type 3A receptor. J Biol Chem, 283 (28): 19301-13. [PMID:18474595]
36. Mair ID, Lambert JJ, Yang J, Dempster J, Peters JA. (1998) Pharmacological characterization of a rat 5-hydroxytryptamine type3 receptor subunit (r5-HT3A(b)) expressed in Xenopus laevis oocytes. Br J Pharmacol, 124 (8): 1667-74. [PMID:9756382]
37. Mazurov AA, Speake JD, Yohannes D. (2011) Discovery and development of α7 nicotinic acetylcholine receptor modulators. J Med Chem, 54 (23): 7943-61. [PMID:21919481]
38. Miyake A, Mochizuki S, Takemoto Y, Akuzawa S. (1995) Molecular cloning of human 5-hydroxytryptamine3 receptor: heterogeneity in distribution and function among species. Mol Pharmacol, 48 (3): 407-16. [PMID:7565620]
39. Mochizuki S, Miyake A, Furuichi K. (1999) Identification of a domain affecting agonist potency of meta-chlorophenylbiguanide in 5-HT3 receptors. Eur J Pharmacol, 369 (1): 125-32. [PMID:10204690]
40. Mochizuki S, Miyake A, Furuichi K. (1999) Ion permeation properties of a cloned human 5-HT3 receptor transiently expressed in HEK 293 cells. Amino Acids, 17 (3): 243-55. [PMID:10582123]
41. Moura Barbosa AJ, De Rienzo F, Ramos MJ, Menziani MC. (2010) Computational analysis of ligand recognition sites of homo- and heteropentameric 5-HT3 receptors. Eur J Med Chem, 45 (11): 4746-60. [PMID:20724042]
42. Newman AS, Batis N, Grafton G, Caputo F, Brady CA, Lambert JJ, Peters JA, Gordon J, Brain KL, Powell AD et al.. (2013) 5-Chloroindole: a potent allosteric modulator of the 5-HT₃ receptor. Br J Pharmacol, 169 (6): 1228-38. [PMID:23594147]
43. Niemeyer MI, Lummis SC. (1998) Different efficacy of specific agonists at 5-HT3 receptor splice variants: the role of the extra six amino acid segment. Br J Pharmacol, 123 (4): 661-6. [PMID:9517385]
44. Niemeyer MI, Lummis SC. (2001) The role of the agonist binding site in Ca(2+) inhibition of the recombinant 5-HT(3A) receptor. Eur J Pharmacol, 428 (2): 153-61. [PMID:11675031]
45. Noam Y, Wadman WJ, van Hooft JA. (2008) On the voltage-dependent Ca2+ block of serotonin 5-HT3 receptors: a critical role of intracellular phosphates. J Physiol (Lond.), 586 (15): 3629-38. [PMID:18566001]
46. Parker RM, Barnes JM, Ge J, Barber PC, Barnes NM. (1996) Autoradiographic distribution of [3H]-(S)-zacopride-labelled 5-HT3 receptors in human brain. J Neurol Sci, 144 (1-2): 119-27. [PMID:8994113]
47. Price KL, Lummis SC. (2005) FlexStation examination of 5-HT3 receptor function using Ca2+ - and membrane potential-sensitive dyes: advantages and potential problems. J Neurosci Methods, 149 (2): 172-7. [PMID:16038983]
48. Roberts A, Grafton G, Powell AD, Brock K, Chen C, Xie D, Huang J, Liu S, Cooper AJ, Brady CA et al.. (2020) CSTI-300 (SMP-100); a Novel 5-HT3 Receptor Partial Agonist with Potential to Treat Patients with Irritable Bowel Syndrome or Carcinoid Syndrome. J Pharmacol Exp Ther, 373 (1): 122-134. [PMID:32102919]
49. Rüsch D, Musset B, Wulf H, Schuster A, Raines DE. (2007) Subunit-dependent modulation of the 5-hydroxytryptamine type 3 receptor open-close equilibrium by n-alcohols. J Pharmacol Exp Ther, 321 (3): 1069-74. [PMID:17360702]
50. Solt K, Stevens RJ, Davies PA, Raines DE. (2005) General anesthetic-induced channel gating enhancement of 5-hydroxytryptamine type 3 receptors depends on receptor subunit composition. J Pharmacol Exp Ther, 315 (2): 771-6. [PMID:16081679]
51. Sun H, McCardy EA, Machu TK, Blanton MP. (1999) Characterization of interaction of 3,4,5-trimethoxybenzoic acid 8-(diethylamino)octyl ester with Torpedo californica nicotinic acetylcholine receptor and 5-hydroxytryptamine3 receptor. J Pharmacol Exp Ther, 290 (1): 129-35. [PMID:10381768]
52. Thompson AJ, Duke RK, Lummis SC. (2011) Binding sites for bilobalide, diltiazem, ginkgolide, and picrotoxinin at the 5-HT3 receptor. Mol Pharmacol, 80 (1): 183-90. [PMID:21505038]
53. van Hooft JA, van der Haar E, Vijverberg HP. (1997) Allosteric potentiation of the 5-HT3 receptor-mediated ion current in N1E-115 neuroblastoma cells by 5-hydroxyindole and analogues. Neuropharmacology, 36 (4-5): 649-53. [PMID:9225290]
54. Walstab J, Combrink S, Brüss M, Göthert M, Niesler B, Bönisch H. (2007) Aequorin luminescence-based assay for 5-hydroxytryptamine (serotonin) type 3 receptor characterization. Anal Biochem, 368 (2): 185-92. [PMID:17617370]
55. Yan D, Pedersen SE, White MM. (1998) Interaction of D-tubocurarine analogs with the 5HT3 receptor. Neuropharmacology, 37 (2): 251-7. [PMID:9680250]
56. Zhou Q, Verdoorn TA, Lovinger DM. (1998) Alcohols potentiate the function of 5-HT3 receptor-channels on NCB-20 neuroblastoma cells by favouring and stabilizing the open channel state. J Physiol (Lond.), 507 ( Pt 2): 335-52. [PMID:9518697]